Antes de empezar, es conveniente dar una ojeada a un clásico del cómic cuyo autor es Carl Basks, “The Big Bin on Killmotor Hill” (“Los caudales congelados”) [1].
Esta es una historieta típica en la que el tío Rico MacPato intenta defender su depósito de dinero de los Chicos Malos (o Golfos Apandadores). Atendiendo una sugerencia del Pato Donald, llena el depósito con agua. Pero lamentablemente aquella noche fatal estaba destinada a ser la más fría en la historia de Patolandia, así es que el agua se congeló y acabó rompiendo los “muros de tres metros” del depósito. Finalmente, el depósito repleto de hielo y de dólares se deslizó por la colina hasta el campamento de los Chicos Malos.

Es un hecho bien conocido que el agua se dilata al congelarse; de hecho, todos hemos sufrido alguna vez esta experiencia que se produce a menudo cuando se intentan enfriar rápidamente las botellas de cerveza o de vino en el congelador (Fig. 1). Además, esta es la razón de que el hielo flote. Pero, ¿por qué se comporta el agua de esta manera?
En primer lugar, tenemos que recordar que el valor de la temperatura se relaciona con la energía cinética de las moléculas, que normalmente tienden a permanecer en una configuración que supone un mínimo de energía (en un escenario clásico). En general, si se adopta un modelo simple de tipo bola de átomos, la configuración de mínima energía es más compacta que una con más energía (y por tanto más desordenada). Pero este no es el caso del agua.
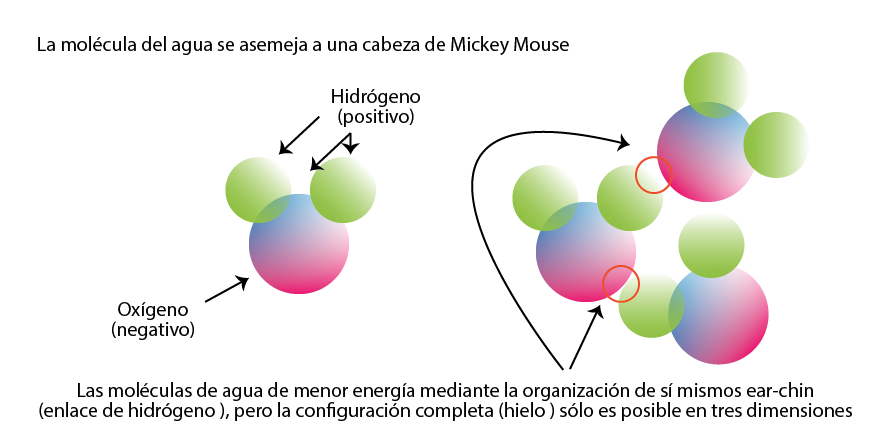
De hecho, las moléculas de agua se asemejan a la cabeza de Mickey Mouse (obsérvese el primer dibujo de la Fig. 2), los dos átomos de hidrógeno serían las orejas. Es difícil dibujar la estructura cristalográfica del agua, ya que se trata de una molécula que solo se puede representar en un retículo en tres dimensiones, pero se puede hacer uso del modelo de “Mercedes Benz” [2]. En este modelo, las moléculas de agua se representan como el famoso símbolo de Mercedes-Benz (Fig. 3), y se obtiene el mínimo de la energía cuando se unen dos espigas (una versión no orientada del enlace de hidrógeno).
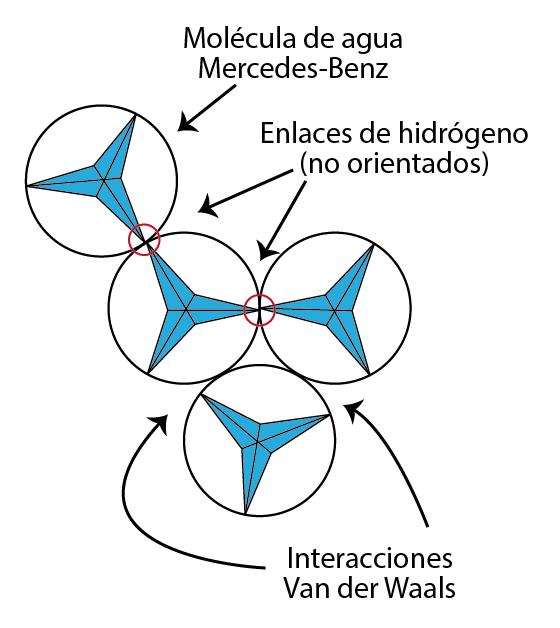
No es demasiado complicado preparar con un poco de cartulina unas moléculas con aspecto “Mercedes-Benz” y hacer el experimento en casa.
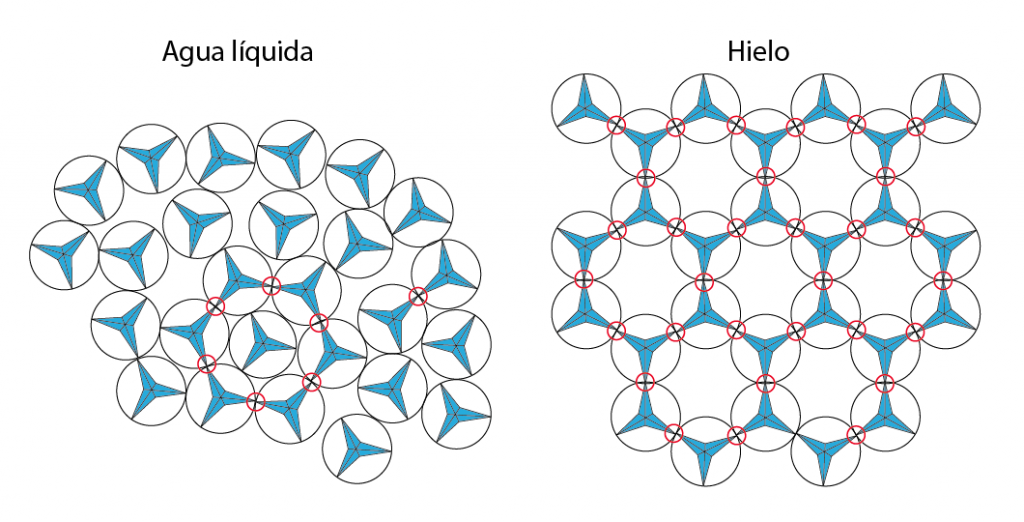
Mediante este modelo es fácil ilustrar que la configuración de energía mínima contiene una gran cantidad de “vacío” (Fig. 4), y esto explica la menor densidad del hielo con respecto al agua. También puede servir para ilustrar el fenómeno de la regelación (que consiste en alcanzar el punto de fusión bajo presión y producir de nuevo congelación al reducir la presión). En realidad, el proceso de la regelación lo podemos ver en casa al presionar un cubo de hielo contra otro: vemos que el hielo en la superficie de contacto se derrite y luego, al dejar de oprimir, el agua entre ellos se vuelve a congelar (uniendo los cubos).
El agua, al congelarse, libera una gran cantidad de calor latente, y más calor todavía debido a su gran capacidad térmica, cuando ya no está a cero grados; entonces difícilmente una noche que se produzca una helada puede congelar el depósito de Rico MacPato lleno de agua [3]>. Pero así son las historietas. C2
Nota: el texto anterior es parte de un seminario presentado por el autor en la “Noche Europea de los Investigadores” en la Universidad de Florencia.
Referencias
[1] Carl Barks, The Big Bin on Killmotor Hill, http://coa.inducks.org/ story.php?c=W+WDC+135-02 (1951). http://it.paperpedia.wikia.com/wiki/File:Big_bin_on_killmotor_hill.pdf
[2] K. A. T. Silverstein, A. D. J. Haymet and K. A. Dill, A Simple Model of Water and the Hydrophobic Efect, J. Am. Chem. Soc. 120, 3166-3175 (1998). doi: 10.1021/ja973029k
[3] http://www.wolfgnards.com/index.php/2009/08/27/how-rich-is-scrooge-mcduck