Este artículo se publicó originalmente en la Revista Avance y Perspectiva del CINVESTAV, Vol. 6 – Núm 1
A manera de introducción
Durante los días transcurridos en esta contingencia sanitaria que nos mantiene aislados en casa, hemos aprendido mucho sobre la biología del SARS-CoV-2, el virus culpable de la Covid-19. Dos excelentes textos que describen los detalles de esta pandemia se publicaron en las páginas digitales de Avance y Perspectiva (1 y 2).
Los lectores que no tienen temor a tecnicismos, pueden consultar decenas de revistas científicas prestigiosas para ahondar en el tema del corona virus. Hay muchísima información. Una búsqueda rápida en la base de datos Scopus de la editorial Elsevier, arroja al día de hoy (22 de mayo 2020) nada menos que 4177 artículos en lo que va del año; 3365 de los cuales son de acceso abierto en revistas de prestigio como Nature Communications, Scientific Reports, PlosOne, Frontiers, etcétera. Del total de artículos publicados, 3508 versan sobre Medicina; 570 sobre Inmunología y Microbiología; 570 sobre Bioquímica, Genética y Biología Molecular; 209 sobre Farmacología; 150 sobre Ciencias del Ambiente; etcétera.
Para mi sorpresa, y sorpresa quizás de muchos lectores perspicaces, vemos que Scopus no reporta ningún artículo de física concerniente al SARS-CoV-2. Mi sorpresa se transforma en vergüenza. Los físicos siempre metemos la nariz en todos lados, creamos modelos y aplicamos leyes para explicar fenómenos de todo tipo, incluso biológicos. ¿Entonces qué nos ocurre, no tenemos esta vez ninguna opinión calificada sobre la pandemia que ha puesto al mundo en esta situación? ¿No entendemos qué cosa es el SARS-CoV-2? ¿No entendemos su forma de actuar? ¿O no nos aventuramos a escribir algo?
La motivación para escribir estas líneas es contribuir con un granito de arena en el mar de información que nos inunda, quizá con el fin de ayudar a comprender, más allá de lo actualmente dicho, al SARS-CoV-2. No hay forma de comprender a cabalidad lo que ocurre con este diminuto patógeno, si no empleamos la física. No soy experto en virus ni mucho menos, pero creo que la física puede ayudarnos a capturar los pormenores del virus. Si los expertos la emplearan, podrían contener al máximo las prisas por publicar resultados incompletos o evitar dar palos de ciego.
¿Palos de ciego o prisas por adquirir fama?
Veamos la polémica mundial desatada por Didier Raoult, destacado microbiólogo francés y director del Instituto Hospital Universitario en Marsella, Francia. A grandes rasgos, Didier Raoult reportó en marzo de este año el uso de una terapia cien por ciento efectiva contra la enfermedad Covid-19. Ésta se basa en el uso de dos fármacos: sulfato de hidroxicloroquina y azitromicina. El primero es ampliamente empleado para tratar malaria, artritis reumatoide y lupus; el segundo es uno de los antibióticos más usados en EU. Con una muy pobre estadística, pues solamente se les administró estos fármacos a 6 pacientes de un total de 36 (de los cuales a 14 se les trató solamente con sulfato de hidroxicloroquina y a 16 con nada), el científico francés, galardonado con el premio Inserm, uno de los más importantes en Francia, con más de 150 mil citas por sus trabajos, publicó sus resultados en una revista científica. Luego defendió su terapia en todos los foros que pudo encontrar.
La crítica a su apresurado trabajo no se hizo esperar. Y ésta vino de sus contrapartes parisinos, que con una muestra de sus propios pacientes no obtuvieron los resultados que pregonaba Raoult. La historia completa se puede leer aquí.
Un reporte sobre la infructuosa terapia acaba de aparecer (hoy 22 de mayo) en la revista Lancet, el cual concluye que después de un estudio con 100 mil pacientes, las drogas propuestas por Raoult no sólo no ayudan en nada, sino son dañinas (aumentan los fallecimientos en lugar de disminuirlos).
Otros intentos para encontrar una terapia se han dado fuera de Francia. Baste recordar la defensa que hizo Donald Trump, no del cloro que recomendó a sus huestes tomar para aniquilar al virus, sino de un medicamento llamado remdesivir. Se reportó que tal sustancia reducía unos días la enfermedad Covid-19 (a 36 de 53 pacientes) y el presidente de Estados Unidos lo defendió a capa y espada.
Los fármacos mencionados pudieran ser útiles para casos muy graves y se debe entender que su uso es compasivo. Pero no para una terapia.
El imaginario popular, representado por charlatanes aquí y en China, no se queda atrás. Propone recetas caseras de todo tipo: una cucharada de aceite de coco por las mañanas; dióxido de cloro; té de limón con aspirinas; sopa de ajo; un vaso de agua con una cucharada de bicarbonato de sodio, etcétera. Algo tiene que matar al enemigo invisible que nos tiene así.
¿Cómo se forma el virus?
Demos un repaso a lo que ya sabemos. La macromolécula que el virus lleva dentro, el ácido ribonucleico o ARN, es el código genético que necesita para hacer múltiples copias de él. Tiene casi 30 mil bases nitrogenadas, también llamadas nucleótidos. Si cada 3 nucleótidos pueden hacer un aminoácido, entonces existe suficiente información para producir 10 mil aminoácidos. Y por ende varias proteínas; entre ellas la más importante, la proteína S, que está constituida por un poco más de mil aminoácidos.
¿Dónde se lleva a cabo la replicación del virus? Dentro de las células de nuestros pulmones. El virus entra en una célula y se adueña de su maquinaria celular para copiarse una y otra vez.
¿Dónde se lleva a cabo la replicación del virus?
Tanto el ARN como las proteínas S, son moléculas con carga eléctrica muy localizada. Regiones positivas y regiones negativas. Podemos decirlo de otra forma: las positivas están protonadas y las negativas deprotonadas. Es el destino de toda molécula que esté disuelta en agua: ganar o perder protones. Y todo depende del pH, que es una medida logarítmica de la concentración de protones en un medio acuoso.
¿Qué ocurre cuando en la sopa interior de una célula hay ARN’s y las proteínas recién hechas del virus? Todo se atrae y se repele, dependiendo de quién se acerque a quién, en qué dirección, y qué compatibilidad eléctrica tengan. Lo negativo se atrae a lo positivo, lo positivo a lo negativo, incluso lo neutro atrae a lo neutro (mediante fuerzas llamadas de dispersión). Todo dictado por la Ley de Coulomb en sus muchas variantes. Al final los ingredientes se agrupan de forma tal que minimizan su energía electrostática. ¿Y qué ocurre con el agua que anda por ahí? Durante el proceso de ensamblado, las moléculas de agua ayudan en la tarea siguiendo una ley llamada Segunda Ley de la Termodinámica. Esta ley nos dice que en cualquier sistema cerrado, la entropía siempre aumenta, así que las moléculas de agua buscan aumentar su entropía o desordenarse lo más que puedan. Al final, todo queda en orden (o en desorden): el virus se auto-ensambla en una partícula que mide 100 nm o una décima de micra y las moléculas de agua a su alrededor maximizan su desorden molecular.
Cuando el virus ya está armado (en su doble acepción: armado de estructurado y armado con sus mortales espinas para infectar), queda listo para continuar dentro de la célula lastimándola o salir y seguir con su ciclo replicativo. Si ocurre lo segundo, otra vez la Segunda Ley de le Termodinámica entra en acción, pero esta vez lo expulsa. Las moléculas de agua que están en su alrededor lo empujan hacia la parte interna de la membrana celular (por fuerzas que justamente se llaman fuerzas entrópicas) para así maximizar su entropía. Dicho de otro modo: a las moléculas de agua no les “gusta” ese extraño ahí y lo arrinconan contra la pared. La célula se libera del virus, y al salir, se lleva consigo lípidos de membranas de órganos celulares internos o incluso de la membrana celular. Por tal razón, el virus tiene una membrana de lípidos, principalmente colesterol y esfingomielina, ver la figura 1. Estos lípidos son muy importantes para su estabilidad e integridad. Sin ellos no podría ser viable. Recuerde el lector que una de las recomendaciones para librarse de él, en caso de que lo tenga adherido a sus manos, es lavarse con jabón. El jabón esta compuesto de moléculas letales para el virus, porque le roba los lípidos. Tal como en la cocina lavamos los platos con jabón para eliminar la grasa (generalmente lípidos).
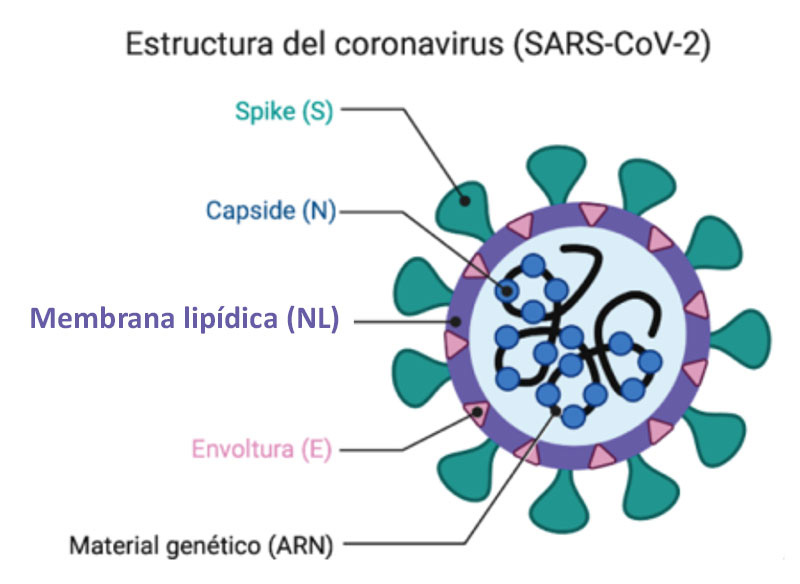
Conclusión 1: el SARS-CoV-2 es una partícula nanométrica que se auto-ensambló dentro de una célula con la única ayuda de dos leyes de la física: la Ley de Coulomb y la Segunda Ley de la Termodinámica.
La infección
Ahora demos un paso atrás en el tiempo y analicemos cuando el virus está en la mucosa de las vías respiratorias. Porque si algo ya sabemos después de tanto encierro leyendo y viendo las noticias, es que lo introducimos a los pulmones al respirar en un ambiente donde hay gotitas minúsculas en el aire con el virus dentro. O lo llevamos a la boca al tocarnos con las manos. Tarde o temprano el virus se adhiere a una célula pulmonar. Hay dos fuerzas que lo obligan a hacerlo. Otra vez la fuerza entrópica y una fuerza electrostática, pero esta vez dipolar. Dipolar viene de dipolo. Un dipolo, como su nombre lo indica, tiene dos polos: uno negativo y otro positivo. Muy pegaditos, generalmente a distancias de un angstrom (1 x 10-10 m).
Por su tamaño, el virus es una partícula extraña en el medio en que esté. Vaga por las vías respiratorias hasta que las moléculas de agua lo arrinconan contra la pared externa de las células. Y en ellas se adhiere por la acción de una fuerza dipolar que tiene su origen en algunos aminoácidos de sus proteínas S. De hecho, las proteínas S tienen dos sub-dominios, el S1 y el S2. En el S1 están tales aminoácidos. Éstos tienen átomos de nitrógeno u oxígeno, que se llaman aceptores de puentes de hidrógeno. O también tienen átomos de hidrógeno de los pares O-H y N-H, llamados donadores de puentes de hidrógeno. Lo mismo ocurre en la enzima ACE2, en las células pulmonares que están en la superficie y que son donde los virus se pegan. Hay aceptores y donadores de puentes de hidrógeno. Entre un aceptor (del dominio S1) y un donador (de la enzima ACE2) (o un donador del primero y un aceptor de la segunda) se establece una interacción dipolar. Igual como el polo sur de un imán atrae al polo norte de otro. De hecho, esta última también es una interacción dipolar, pero magnética.
El virus se sujeta con fuerzas dipolares a la célula que después va a infectar.
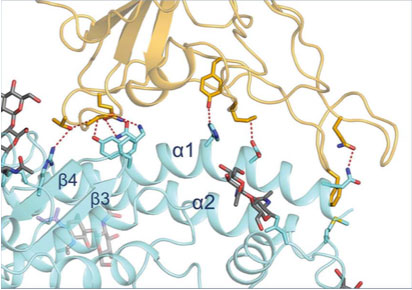
En un artículo reciente Renhong Yan y colaboradores analizan las interacciones dipolares entre uno de los aminoácidos del dominio S1 de la proteína S y la enzima ACE2: estructura amarilla y azul, respectivamente, en la figura 2. Las líneas punteadas representan los enlaces de puente de hidrógeno. Las terminaciones rojas son aceptores y las azules donadores.
Los biólogos hablan normalmente de un mecanismo conocido como llave-cerradura. Se refieren a que un ligando (por ejemplo, un aminoácido del virus actual) es una muesca de la llave. Siendo la cerradura uno o varios aminoácidos de la proteína de una célula. Es una forma coloquial o metafórica para describir la interacción que ocurre, pero debemos saber que aquí no hay una llave abriendo una cerradura. Lo que hay son interacciones electrostáticas específicas bien definidas. Además, una vez que la llave entra a la cerradura, ¿quién le da vuelta a la chapa de la puerta?
Conclusión 2: un virus que entró a nuestro cuerpo y llegó a una célula de los pulmones, se adhiere mediante interacciones electrostáticas dipolares a la enzima ACE2.
Lo que ocurre a continuación sigue siendo parte del juego electrostático. Ahora entra en juego el dominio S2 de la proteína S del virus. En él hay aminoácidos hidrofóbicos. Están escondidos dentro porque no les gusta el agua que hay por todos lados, en los mocos o en las gotitas de saliva. Éstos “ven” que en la membrana de la célula a la que llegaron también hay una zona hidrofóbica, formada por las colas hidrocarbonadas de los lipídos que componen la membrana. Entre los aminoácidos hidrofóbicos del dominio S2 y la zona hidrofóbica de la membrana, entra en acción una fuerza llamada de van der Waals o de dispersión. Se requerirían varias páginas para explicar bien su origen, pero baste decir que es una fuerza atractiva de corta distancia. El agua es líquida por culpa de puentes de hidrógeno (las moléculas de agua se unen entre ellas mediante estos puentes); el aceite de oliva es líquido por fuerzas de van der Waals. Estas fuerzas son también dipolares, pero promediadas porque los dipolos aparecen y desaparecen trillones de veces en un abrir y cerrar de ojos.
Cuando la pobre célula, sin saber que se instalarán en su cuarto de cómputo sin permiso, engulle al virus con todo y sus espinas, como quien invita a un lobo disfrazado de oveja, hay un cambio de elasticidad en su membrana. Todo orquestado por una danza dipolar eléctrica.
Resumiendo: con este zambullido van-der-Waalsiano (o endocitosis), el virus se mete en la célula hasta la cocina, saca su USB o ARN, lo conecta a la computadora de la célula y empieza a copiarse por miles. Para mala suerte nuestra.
¿Qué tanto es tantito?
Según Daniel Wrapp y colaboradores (ver aquí), la constante de afinidad entre los dos dominios representados en la figura 3, es de 15 nM (nano molar). ¿Qué significa este valor? Indica que para garantizar una unión eficiente (digamos aquella que da lugar a una infección) entre los aminoácidos del dominio S1 de la proteína S del virus y los aminoácidos de la enzima ACE2 de la célula, se requieren diez mil millones de millones de uniones de este tipo (valor que resulta al multiplicar 15 x 10-9 por el número de Avogadro 6 x 1023). Para tener una referencia, veamos el anterior corona virus que causó la pandemia de 2002 (el SARS-CoV-1): la constante de afinidad entre sus proteínas S y la enzima ACE2 es de 6.5 µM (ver aquí). Comparando las afinidades, podemos ver que el corona virus culpable del Apocalipsis actual, el SARS-CoV-2, es 433 veces más infectivo que el SARS-CoV-1.
La constante de afinidad kD se define como kD = exp[(Gf-Gi)/RT] (donde Gf, Gi, R y T son la energía libre final, energía libre inicial, constante de los gases y temperatura en Kelvin, respectivamente). Así que el cambio en la energía libre (Gf-Gi) del virus cuando infecta a una célula a la temperatura fisiológica (310 K), es de -11.1 kcal/mol. Cabe señalar que un cambio negativo en la energía libre denota una ligadura favorable entre un ligando y un receptor. En este caso el ligando es el dominio S1 de la proteína S del virus y el receptor la enzima. El cambio en la energía libre de -11.1 kcal/mol es un tanto por el cambio en la entalpía debido a la unión entre aminoácidos y otro tanto por el aumento en la entropía del agua. La constante de afinidad de 6.5 µM del SARS-CoV equivale a un cambio de energía libre de -7.35 kcal/mol. Existe una diferencia de -3.75 kcal/mol entre ambos virus. En términos de energía, el SARS-CoV-2 se adhiere a la enzima ACE2, 3 veces más fuerte que el SARS-CoV-1.
Es importante señalar que aunque el SARS-CoV-2 es 433 veces más óptimo o infectivo que el SARS-CoV-1 (explicándose así la frenética propagación de la Covid-19 con respecto a la que aquejó a la humanidad con el SARS-CoV-1), la mortalidad es mucho menor. De hecho, el porcentaje de fallecimientos por el SARS-CoV-2 está entre 2 y 3%, mientras que con el SARS-CoV-1 fue del 10%. Es decir, 433 veces más infectivo, pero menos letal.
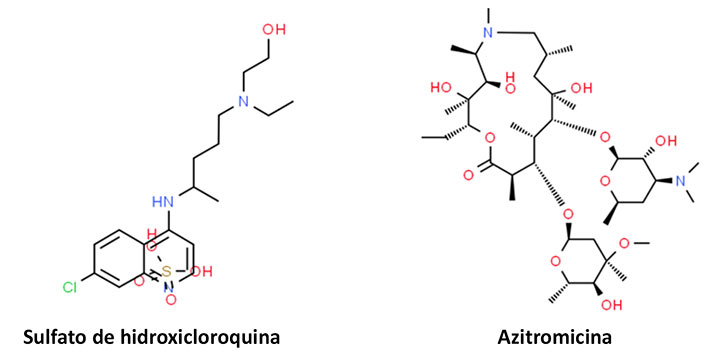
Arriba señalé que muchas personas (científicos y legos), en la búsqueda de un remedio contra la Covid-19, dan palos de ciego. Veamos si no. En la figura 3 se muestran las moléculas de sulfato de hidroxicloroquina y azitromicina, los ingredientes del elixir propuesto por el científico francés Didier Raoult. Si ingerimos estas dos moléculas juntas, como propone el microbiólogo francés, estaremos tomando una buena dosis de aceptores y donadores de puentes de hidrógeno, nada menos que 21 y 9, respectivamente (por cada par de moléculas ingeridas). Cuente el lector los oxígenos, nitrógenos e hidrógenos, para corroborar estos números.
Desde luego que esta poción inhibirá al virus, pues sus aceptores/donadores se pegarán como imanes a los donadores/aceptores de sus aminoácidos. Y así, el virus ya no podrá unirse a la enzima ACE2. Es como si al virus le ponemos unos guantes (o dedales en sus dedos) para que no se pueda agarrar con sus uñas a nada. Asunto arreglado. Final feliz. Por eso los seis pacientes del científico francés se curaron de la neumonía que les produjo el SARS-CoV-2
Pero también entendemos por qué los pacientes de los médicos parisinos empezaron a enfermarse del corazón, hígado e intestinos. Y vaya usted a saber de qué más. Los aceptores/donadores de puentes de hidrógeno de las drogas no hacen distingos. Van y se unen a cuanta contraparte dipolar encuentren aquí y allá. Es decir, esas drogas que ahora hasta Trump toma por si las dudas (como nos enteramos el 19 de mayo), no son específicas al virus. Agarran parejo, o más bien se agarran a todo. Porque para estas alturas, al lector le debe de quedar claro que TODAS las células de nuestro cuerpo tienen aminoácidos con aceptores y donadores de puentes de hidrógeno. El destino de lo que nos tomemos por vía oral o intravenosa, que entre a nuestro cuerpo y vague por la mucosa o sangre, irremediablemente encontrará su contraparte dipolar eléctrica y se pegará. No hay más, la electrostática domina lo que ocurre cuando ingerimos algo y circula por nuestras entrañas.
Más infeccioso, menos mortal
Para finalizar, veamos por qué el SARS-CoV-2, que es más infectivo que el SARS-CoV-1, es menos fatal. La hipótesis es que una mutación, en el SARS-CoV-1, creó más aceptores/donadores de puentes de hidrógeno y de ahí derivó el SARS-CoV-2. Y justamente porque se trata de un virus óptimo, el sistema inmune, que produce en forma natural anticuerpos para inhibir al virus, tiene la tarea más fácil. En la eficiencia está su perdición: así como el SARS-CoV-2 es óptimo como ligando, es también óptimo como receptor (de un anticuerpo). Si nuestro sistema inmune está al cien, este lo inactiva en un dos por tres. Unas por otras.
Me atrevo a decir que la vacuna que con ansia estamos esperando, no tardará en llegar. Justamente porque el SARS-CoV-2 es mucho mejor ligando, y por ende óptimo receptor, una vacuna que logre hacer trabajar nuestro sistema inmune, tendrá la fácil tarea de producir ligandos (anticuerpos) para inhibirlo. Crucemos los dedos.
Agradezco a la Dra. Ana Lorena Gutierrez Escolano por sus comentarios y correcciones a este texto. C2













BLANCA DOMINGUEZ -
Excelente ¡¡¡¡¡¡¡¡¡¡¡¡