De acuerdo a la Federación Mexicana de Diabetes, más de 6 millones de personas padecen de diabetes en nuestro país.
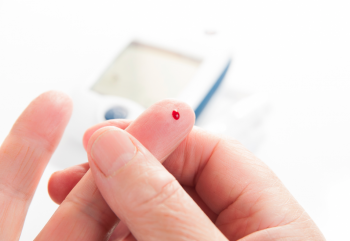
La mayoría de estas son tipo 1: necesitan de un tratamiento personalizado en el cual una dosis de insulina es suministrada dependiendo del nivel de glucosa del paciente. Afortunadamente existen los glucómetros, que son aparatos que caben en la palma de la mano y que permiten al propio paciente monitorear sus niveles de glucosa a partir de una gotita de sangre. De esta manera, la calidad de vida del paciente diabético no se ve modificada en gran medida. El glucómetro, ejemplifica a la perfección el concepto de un biosensor: un dispositivo portátil que detecta y mide la cantidad de una sustancia de interés (drogas, proteínas, virus, bacterias, ADN, etc…) de manera precisa, rápida, simple y económica.
¿Por qué no existen biosensores comerciales para detectar Ebola, influenza, cáncer, VIH u otro tipo de padecimiento?
En este punto, el lector podría preguntarse, dadas las ventajas que los biosensores brindan al diagnóstico y tratamiento médicos: ¿por qué no existen biosensores comerciales para detectar Ebola, influenza, cáncer, VIH u otro tipo de padecimiento que también afecte a gran parte de la población mundial? La glucosa puede ser detectada fácilmente debido a que se encuentra en una gran cantidad en una muestra de sangre, lo cual facilita la detección por medio de una reacción electroquímica. Sin embargo, la detección de la sustancia de interés (también llamada analito) se complica cuando se encuentra en cantidades reducidas, digamos, ¡miles de millones de veces menor que la concentración de glucosa! Más aun, tengamos en cuenta que las muestras biológicas como la sangre o la saliva son sustancias complejas que contienen una infinidad de otras proteínas y células que en conjunto pueden enmascarar la señal proveniente del analito.
 La glucosa puede ser detectada fácilmente debido a que se encuentra en una gran cantidad en una muestra de sangre, lo cual facilita la detección por medio de una reacción electroquímica. Un razonamiento inmediato ante esta limitante es, entonces, la necesidad de aislar y concentrar a determinado analito de la muestra total. ¿Cómo lograr esto en el interior de un biosensor? Una de las estrategias se basa en el uso de perlas superparamagnéticas que son diminutas [1] y que están hechas a base de poliestireno y magnetita (Fe3O4). Estas presentan una dualidad especial: pueden ser magnéticas o no-magnéticas, dependiendo de si se aplica un campo magnético o no, respectivamente. Estas partículas también pueden ser modificadas con distintos grupos químicos para adherir biomoléculas.
La glucosa puede ser detectada fácilmente debido a que se encuentra en una gran cantidad en una muestra de sangre, lo cual facilita la detección por medio de una reacción electroquímica. Un razonamiento inmediato ante esta limitante es, entonces, la necesidad de aislar y concentrar a determinado analito de la muestra total. ¿Cómo lograr esto en el interior de un biosensor? Una de las estrategias se basa en el uso de perlas superparamagnéticas que son diminutas [1] y que están hechas a base de poliestireno y magnetita (Fe3O4). Estas presentan una dualidad especial: pueden ser magnéticas o no-magnéticas, dependiendo de si se aplica un campo magnético o no, respectivamente. Estas partículas también pueden ser modificadas con distintos grupos químicos para adherir biomoléculas.
Los biosensores a base de perlas magnéticas emulan el mecanismo de nuestro sistema inmune en el que los anticuerpos, producidos por los linfocitos, reconocen de manera altamente específica un agente externo (también llamado antígeno). Del mismo modo, cuando las perlas magnéticas son recubiertas con anticuerpos, pueden ser usadas para capturar antígenos. La captura de antígenos puede ser acelerada utilizando diferentes protocolos de agitación magnética. Una vez que el antígeno es anclado a la muestra este puede ser aislado, purificado y transportado a un dispositivo (chip), de nuevo echando mano de los campos magnéticos. Más aún, las partículas magnéticas, debido a su tamaño en comparación al tamaño del analito, pueden ser fácilmente detectadas por métodos ópticos. De esta manera el rendimiento de un biosensor puede ser amplificado.
Dicho prototipo se encuentra en la fase de desarrollo comercial y ayudara a pacientes propensos a la detección oportuna de ataques cardiacos.
Varios grupos de investigación se encuentran desarrollando prototipos de sensores basados en partículas magnéticas [2]. Por ejemplo, usando una plataforma ópto-magnética, Bruls y colaboradores [3], lograron detectar la proteína Troponina I, la cual es el principal indicador de fallas cardiacas. El dispositivo consiste en un sistema de componentes eléctricos que pueden generar campos magnéticos de manera controlada y sistemática. De una muestra de plasma sanguíneo, la proteína cardiaca adherida a las perlas magnéticas por medio de un anticuerpo específico. Las partículas son transportadas después a una superficie que contiene un segundo anticuerpo que detecta otra región de la proteína, de tal suerte, que un ensayo tipo “sándwich” es formado (la proteína se encuentra entre una superficie y la partícula magnética). Posteriormente, un gradiente de campo magnético es aplicado para separar las partículas que no están adheridas. En este caso, el número de partículas unidas a la superficie puede ser detectado ópticamente y relacionado con la concentración de Troponina I de la muestra. Dicho prototipo se encuentra en la fase de desarrollo comercial y ayudara a pacientes propensos a la detección oportuna de ataques cardiacos.
Eventualmente, el uso de biosensores revolucionará el sistema de salud hasta ahora existente y permitirá a los médicos tomar mejores decisiones en el diagnóstico y tratamiento del paciente. C2
Referencias
[1] de 100 nanómetros a 3 micrómetros (el diámetro de un cabello humano es 100 micrómetros aproximadamente)
[2] La red de investigadores BioMax desarrolla diferentes ensayos biológicos basados en partículas magnéticas, mayor información en http://www.biomax-itn.eu/
[3] Bruls et al. (2009) Lab o a chip. 9, 3504-3510

enrique rodriguez diaz -
Hola aca tenemos un equipo luminex 200 pero hemos tenido problemas con las perlas para activarlas despues de montadas las pruebas nos da resultados que infieren que las perlas se deben mover mas ,las hemos puesto con un equipo ultrasonico y algunas han dado bien pero otras no que debemos hacer para que se activen correctamente gracias