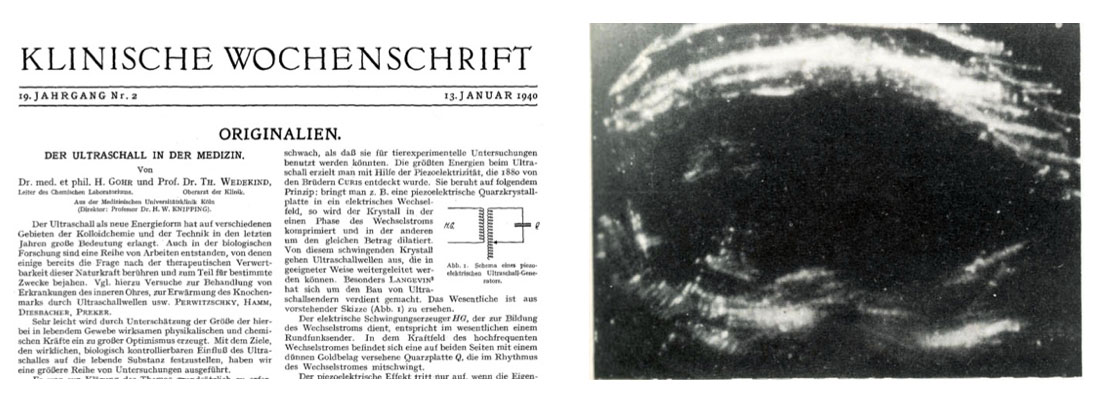
El ultrasonido (US) se ha convertido en una herramienta muy útil de diagnóstico médico. Para el 2016, Smith-Bindman et al. [1] estimaron que el ultrasonido médico rebasaba los 800 estudios por 100 personas-año en los Estados Unidos, convirtiéndolo en la modalidad de imagen más usada comparada con resonancia magnética, tomografía computada por rayos X y medicina nuclear. Hoy en día las imágenes adquiridas con esta modalidad son de muy alta resolución, además de que se puede medir el flujo sanguíneo utilizando el efecto Doppler. Debido a que la adquisición de imágenes es rápida sólo se pueden hacer películas de varios segundos con los equipos de ultrasonido. El desarrollo del ultrasonido médico inicia en la década de los 40 del siglo pasado cuando Gohr y Wedekind proponen que el ultrasonido se puede utilizar para el diagnóstico. No es hasta la década de los 50 que se obtienen las primeras imágenes obstétricas con US [1,2]. En la Figura 1 mostramos una copia de uno de los primeros artículos de ultrasonido médico, así como la primer imagen obstétrica obtenida por Donald en 1958 [3].
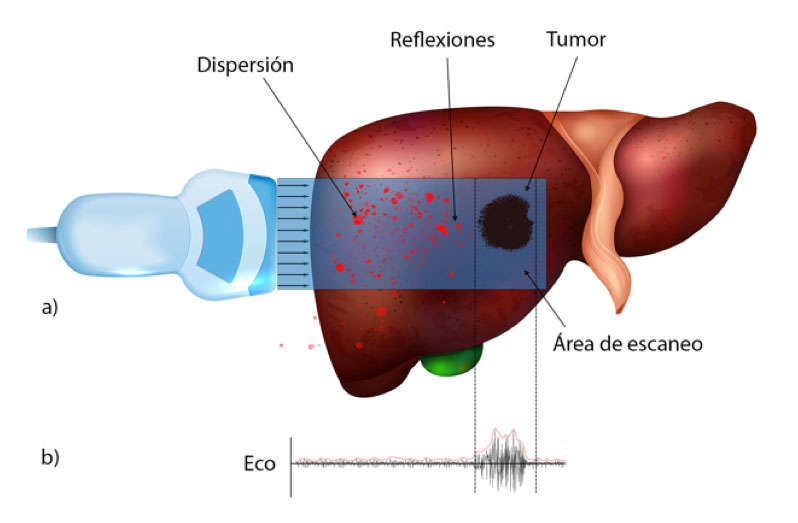
A diferencia de los equipos de rayos X, de resonancia magnética, y de medicina nuclear que se basan en la emisión y/o detección de radiación electromagnética, los equipos de ultrasonido médico utilizan ondas acústicas basadas en oscilaciones de presión del medio en el que viajan. Las oscilaciones son extremadamente rápidas: su frecuencia está por encima del millón de ciclos por segundo o 1 mega Hertz (1 MHz). En comparación, el ser humano promedio puede escuchar ondas sonoras con frecuencias entre 20 y 20 mil ciclos por segundo (20 Hz a 20 KHz). Un equipo clínico de ultrasonido cuenta con varios elementos, como el monitor, teclados, unidad de cómputo; por mucho, el elemento más importante es la sonda o transductor, el cual es un dispositivo que emite la onda de ultrasonido al cuerpo y detecta los ecos producidos por los órganos y tejidos dentro del cuerpo. La modalidad de imagen por ultrasonido más común, la ecografía, funciona de manera similar al radar de los aviones o el sonar de los submarinos: se basa en transmitir una onda corta (del orden de microsegundos) y esperar los ecos producidos por diferentes estructuras y tejidos a diferentes profundidades dentro del cuerpo. Sencillo: mando pulsos y espero los ecos. Así se va realizando un mapeo de la región de estudio y por medio del procesamiento electrónico de cada pulso recibido se obtiene el nivel de color correspondiente a cada pixel dentro de una imagen. Con los sistemas de US es posible medir los tiempos de regreso y la energía de los ecos. Es decir, para construir la imagen se necesita conocer la velocidad del sonido, la dirección en la que se envió el pulso, los tiempos de detección, y la energía recibida de los ecos. En la Figura (2) mostramos un esquema del funcionamiento del US así como la señal o eco recibido [4].
La versatilidad y accesibilidad del ultrasonido médico es una navaja de doble filo: la generación de imágenes y su interpretación es altamente dependiente de quién opere el equipo y de la experiencia del evaluador en interpretar las imágenes. En particular, los equipos de ultrasonido ofrecen una gran cantidad de parámetros de operación que pueden generar imágenes diferentes del mismo tejido. De aquí la pregunta: ¿Cuándo dos imágenes de ultrasonido de una misma estructura son iguales?
Aunque parece una pregunta extraña, en ultrasonido médico esta pregunta es válida. Si dos operadores toman imágenes distintas del mismo órgano o del mismo tejido del mismo paciente, ¿el tejido u órgano se ven iguales? O bien si un operador toma dos imágenes del mismo paciente con dos equipos diferentes, ¿el tejido se ve igual? La respuesta es: no necesariamente. La orientación del transductor con respecto al tejido de interés puede variar de operador a operador. Además, cada operador puede ajustar los parámetros de operación del equipo de diferente manera. Aunado a esto, equipos de diferentes modelos y/o diferentes fabricantes usan algoritmos propios de procesamiento de imágenes para resaltar ciertas características que puedan asistir en su interpretación . El ultrasonido cuantitativo (QUS, por sus siglas en inglés) busca reducir dicha variabilidad a través de cuantificar propiedades físicas inherentes al tejido e independientes de los parámetros de operación y las técnicas de pos-procesamiento [https://doi.org/10.1063/9780735423558_004].
La idea de QUS surge hace aproximadamente 50 años, y se basa en la premisa de que el contenido de frecuencias de las señales de los ecos detectados posee información de las propiedades acústicas (PA) del tejido: velocidad de propagación, atenuación (razón de pérdida de energía con la profundidad) y retrodispersión (reflectividad del tejido). Lo interesante es que dichas PA cambian dependiendo del estado del tejido: si es sano o presenta alguna lesión o proceso patológico, o si cambia como respuesta a un tratamiento. Ejemplifiquemos esto. Una o un radiólogo adquiere la imagen del hígado de un paciente. Si hay exceso de grasa en el hígado, la apariencia del hígado es diferente a la del hígado sano. Para determinar cuánta grasa esta infiltrada en el hígado es necesario hacer una biopsia o un estudio de resonancia magnética. La pregunta es: A partir de la medición de las PA mediante QUS, ¿es posible determinar la cantidad de grasa sin necesidad de una biopsia? La velocidad del sonido y la absorción del hígado sano son distintos al de hígado graso. Entonces, a medida que hay infiltración de grasa las PA cambian, haciendo posible relacionar dichos cambios con la cantidad de grasa. Es decir, el propósito del ultrasonido cuantitativo es pasar de la interpretación cualitativa clínica de las imágenes a la cuantificación.
Otro ejemplo es el uso de QUS para la caracterización de la malignidad de lesiones en la glándula mamaria. ¿Por qué las propiedades acústicas estarían correlacionadas con la malignidad de una lesión cancerosa? Una explicación parcial es que cuando se forma una lesión en mama a su alrededor se distribuyen de manera distinta las fibras de colágeno por lo que pueden ser un indicador o marcador de la evolución del cáncer en un paciente o su malignidad.[https://doi.org/10.1016/j.ajpath.2010.11.076] La distribución del colágeno cambia las propiedades acústicas y la suposición de nuevo es que el cambio de las PA puede ser un biomarcador que nos de información útil en la clínica sobre un tumor. De esta forma, el ultrasonido cuantitativo puede complementar otras técnicas de imagen cuantitativa, como la mastografía por energía dual, la resonancia magnética con medio de contraste, entre otras. Referimos al lector al artículo sobre densidad mamaria [5] utilizando mamografía convencional.
Dentro de las técnicas de ultrasonido cuantitativo, también se considera la elastografía que consiste en poder medir las propiedades elásticas de tejido utilizando la excitación de ondas de corte o cizalla de baja frecuencia (alrededor de cientos de Hz). La idea de la elastografía es obtener propiedades como el módulo de Young y estudiar los cambios dependiendo de alguna condición fisiológica. Regresando al ejemplo del hígado, grados avanzados de infiltración grasa pueden generar fibrosis o el depósito de colágeno dentro del tejido del hígado. Dicha deposición de colágeno aumenta la dureza del tejido, cambio que puede ser detectado y monitoreado por la elastografía. Dentro de QUS la idea es que por medio de un estudio de ultrasonido se puedan obtener valores cuantitativos de la rigidez y utilizarlos para establecer el grado de fibrosis de la o el paciente.
Desde el punto de vista físico, cualquier tejido es altamente inhomogéneo, lo que complica el análisis de la retrodispersión de las ondas de ultrasonido.. Esto hace que la modelación matemática de la propagación de pulsos sea complicada y se base en teorías de dispersión muy parecidas a las utilizadas en física nuclear, como la ecuación de Lippmann-Schwinger pero adaptada al caso acústico involucrando la solución de ecuaciones integro-diferenciables. En el caso de la elastografía, el entendimiento de la propagación de las ondas de cizalla para la extracción de propiedades elásticas del tejido requiere de conocimiento profundo de mecánica de medios continuos y de reología. Dicha complejidad hace que el campo de ultrasonido médico cuantitativo presente retos interesantes para campos del conocimiento como computación, física, ciencias de materiales y matemáticas aplicadas, además de la necesaria colaboración con los médicos de distintas especialidades, como los radiólogos, ginecobstetras, cardiólogos, entre muchos otros. Esto hace del ultrasonido médico y en general de la física médica un área muy interdisciplinaria.
El ultrasonido médico cuantitativo es una herramienta que complementa las imágenes para diagnóstico. Pese a tener casi 50 años de desarrollo, las capacidades computacionales actuales de los sistemas de ultrasonido hacen posible aplicar esta técnicas en la clinica. En México, el Laboratorio de Ultrasonido Médico desarrolla técnicas de QUS y explora su aplicación para el abordaje de diferentes enfermedades, como el cáncer de mama (en colaboración con el Instituto Nacional de Cancerología) y estrés respiratorio neonatal (en colaboración con el Instituto Nacional de Perionatología).
Agradecemos el apoyo del Proyecto de Frontera CONACyT 1311307.
REFERENCIAS
[1] Smith-Bindman R, Kwan ML, Marlow EC, Theis MK, Bolch W, Cheng SY, Bowles EJ, Duncan JR, Greenlee RT, Kushi LH, Pole JD. Trends in the use of medical imaging in US health care systems and Ontario, Canada, 2000-2016. Jama, 322, 2019.
[2] Bodelon C, Mullooly M., Pfeiffer R. M., Fan S., et al. Mammary collagen architecture and its association with mammographic density and lesion severity among women undergoing an image-guided breast biopsy, Breast Cancer Research, 23 (105) 2021.
[3] Donald I, MacVicar J, Brown TG. Investigation of abdominal masses by pulsed ultrasound. Lancet, 1, 1958.
[4] Szabo TL. Diagnostic ultrasound imaging: inside out. Academic Press; 2004.
[5] Pacheco G., Brandan, M. E., Densidad Mamaria ¿Riesgo a simple viste?, Avance y Perspectiva, 8 (2), (2022).