Viene de la parte 1
En la tabla 2 se muestran algunos de los avances que ha tenido el desarrollo de las vacunas (Acheson N, 2009).
Tabla 2. Avances tecnológicos que apoyan el desarrollo de vacunas virales
| 1850 | En Alemania se utilizó glicerina para estabilizar y descontaminar la vacuna de la viruela. |
| 1879 | Víctor Galtier realizó con éxito la transferencia del virus de la rabia de perro a conejo y de conejo a perro. |
| 1884 | Elías Metchnikoff describe el rol de patogénesis en inmunidad. |
| 1885 | Louis Pasteur y colegas descubren que la virulencia del virus de la rabia se pierde durante el secado. |
| 1887 | Julius Richard Petri descubre las placas de vidrio superpuestas para el uso de cultivos estériles. |
| 1897 | Friedrich August Johannes Loeffler y Paul Frosch describen “los virus filtrables” (enfermedad viral de boca y pie). |
| 1931 | Ernest Goodpasture usa por primera vez huevos embrionarios para cultivos virales. |
| 1936 | Wendell Meredith Stanley aísla el ácido nucleico del virus mosaico del tabaco. |
| 1950 | John Franklin Enders, Thomas Huckler Weller y Frederick Chapman Robbins realizan los primeros estudios del cultivo celular con el virus de la poliomielitis. |
| 1953 | George Otto Gey y Mary Kubicek descubren la primera línea celular de células cancerígenas inmortales (HeLa). |
| 1960 | Producción de virus de la Influenza A en huevos de gallina. |
| 1972 | Primer ADN insertado artificialmente en un genoma de bacteria. |
| 1974 | Primera glicoproteína viral recombinante generada en bacterias. |
| 1985 | El gen del antígeno de superficie de la Hepatitis B es insertado en otro DNA para producir proteínas del virus. Se empiezan a utilizar DNA virales como el virus Vaccinia y el virus Herpes Simple para expresar antígenos provenientes de agentes infecciosos y que pueden servir como vacunas. |
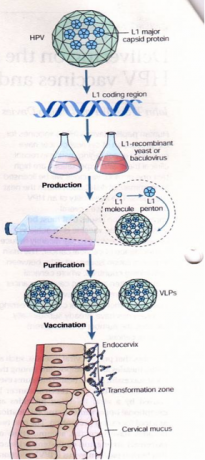
En las últimas décadas se han desarrollado partículas llamadas virosomas, las cuales tienen una forma cuasi esférica, una bicapa membranal con proteínas (glicoproteínas) insertadas que son producidas dentro la célula infectada mediante instrucciones del genoma viral. Cuando la cápside (envoltura proteica del genoma viral) del virus sale de la célula, se lleva parte de la membrana celular que contiene sus propias glicoproteínas, las cuales le sirven para el reconocimiento celular. Los virosomas carecen del genoma viral y pueden ser capaces de producir una respuesta inmune protectora, como en el caso de la vacuna de la Hepatitis B. Hoy en día, los virosomas se pueden sintetizar en grandes cantidades por métodos de biología molecular, donde las glicoproteínas obtenidas de esta manera se conocen como proteínas recombinantes. Los virosomas han sido producidos no solamente para vacunas o terapias virales, sino también como acarreadores de proteínas y genomas para terapia de genes.
A través de los años se han ido desarrollando vacunas contra numerosos agentes infecciosos, desde la inoculación de los virus en animales para producir el virus (para purificar su membrana que contiene las glicoproteínas necesarias para generar la vacuna contra ese virus en particular), hasta, actualmente, la producción de las mismas glicoproteínas por medio de métodos biomoleculares, los cuales son más seguros (al no utilizar el virus) para obtener grandes cantidades de éstas y abastecer gran parte de la población mundial. En la década pasada, ciertos procedimientos moleculares han permitido el desarrollo de vacunas basadas en la tecnología de ADN recombinante, incluyendo bacterias o vectores virales como adenovirus que expresan antígenos de diferentes especies, para la producción de una inmunidad protectora. Las técnicas de cultivo de células, producción de anticuerpos, cristalografía de rayos X y la creación de animales genéticamente modificados ha favorecido un gran adelanto en el campo de las vacunas, sobre todo para las pruebas preliminares in vitro e in vivo de las vacunas antes de probarse en humanos.
No obstante, a pesar de grandes avances tecnológicos, algunos virus como el de la influenza aviar H5N1, persisten
No obstante, a pesar de grandes avances tecnológicos, algunos virus como el de la influenza aviar H5N1, persisten y siguen causando pandemias en animales en muchas partes del mundo. Hay pocos casos de infecciones por este virus en humanos, pero la tasa de mortalidad es muy alta (33-70%). La producción de cambios impredecibles en los genes, llamadas mutaciones, pueden conducir a un contagio en humanos. Además, los virus son altamente patogénicos en las aves y pueden rápidamente matar las células de sus embriones e inhibir su reproducción, lo cual en aves domésticas puede tener consecuencias económicas importantes. Existe una vacuna contra la influenza estacional en humanos y una recombinante aprobadas por la FDA (Food and Drug Administration, USA), pero las vacunas, como en el caso de la influenza, necesitan mejorarse para disminuir las tasas de mortalidad prevalentes. Las investigaciones siguen en curso para el desarrollo de otra vacuna recombinante contra un brote de Influenza H7N9 (Vaccine Technology V, 2015).
En la actualidad se han desarrollado programas como el sistema MIMIC que simula la inmunofisiología de neonatos, adultos, personas en edad avanzada y con alergias. Puede ser usado para examinar no sólo la inmunogenicidad, sino también la funcionalidad de varios fármacos. Adicionalmente, existen programas para el manejo de datos, análisis de proteínas, mapeo de antígenos o epítopes en células inmunes para el diseño previo de vacunas. También, se han creado los nanoparches, que contienen un arreglo o circuito altamente denso de epítopes. Aquí es depositada la proteína recombinante seca, la cual puede ser liberada a través de la piel, vía epidermis y dermis, donde se encuentran gran cantidad de células inmunes, presentadoras de antígenos, capaces de captar y procesar estas proteínas. En ratones, se ha demostrado que estos nanoparches producen una gran cantidad de anticuerpos tipo Inmunoglobulina G que neutralizan al antígeno. Se han desarrollado compuestos llamados bisfosfonatos, que son fármacos cuyo blanco son las células B inmunes y producen una expansión de las mismas con producción de anticuerpos con el antígeno de interés. Estos son una clase de adyuvantes que estimulan la respuesta inmune humoral, es decir, la respuesta inmune relacionada con la producción de anticuerpos (Vaccine Technology V, 2015).
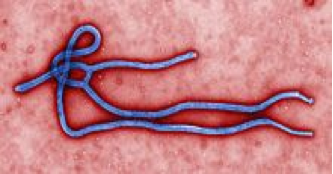
El reto aún sigue para el desarrollo de estrategias que nos permitan erradicar problemas actuales causados por algunos virus y bacterias como son: la Inmunodeficiencia adquirida (VIH), la tuberculosis, la influenza y, más recientemente, el virus del Ébola. De este último se conoce muy poco, pero se sabe que se transmite de persona a persona por un virus perteneciente a la familia de los filovirus; causa fiebre aguda y síndrome hemorrágico generalizado, conduciendo la mayoría de las veces a la muerte (Geisbert TW, 2009). Estudios de comparación se han realizado con los brotes en ciudades y pueblos para generar un esquema de detección y control del esparcimiento del virus (Allaranga Y, 2010). Por otro lado, en primates no humanos -monos- se han desarrollado varios intentos de producir vacunas contra diferentes cepas del virus del Ébola (Geisbert TW, 2009).
Algo que ya está demostrado es que la agresividad del virus es atribuida parcialmente a la proteína de superficie del virus…
Productos antivirales como el BCX4430 que inhibe la actividad de la enzima RNA polimerasa, que es una proteína del virus, produce protección cuando se ha administrado 48 horas después de la infección. Los tratamientos basados en ácidos nucleicos, vacunas recombinantes y anticuerpos, parecen ser menos adecuados para las fiebres hemorrágicas de Marburg y Ébola (Warren TK, 2014). Situaciones de emergencia han hecho que se administren tratamientos como es el caso del fármaco Zmapp, aún no aprobados por la FDA, que han demostrado eficacia previa en no-primates y que fueron administrados a 2 sujetos norteamericanos trabajadores de la salud que actualmente se encuentran libres del virus (Zumbrun EE, 2014). Algo que ya está demostrado es que la agresividad del virus es atribuida parcialmente a la proteína de superficie del virus, llamada sGP; ya que es secretada y fácilmente detectada en personas infectadas, de tal forma que las estrategias para combatir esta epidemia pueden ir enfocadas a diseñar vacunas y tratamientos para bloquear la proteína de superficie del virus (De la Vega, 2015).
El mayor obstáculo en el desarrollo de las vacunas es la incapacidad para entender una protección natural, por lo que investigando más para comprender la patogénesis y los mecanismos que nos confieren protección, nos permitirá continuar en la batalla contra las infecciones; así como la realizaron nuestros antepasados con el virus de la viruela y otros más. Aunque la batalla contra los virus y las bacterias ha ganado terreno, tenemos que tomar en consideración el cambio continuo de los virus y las bacterias a través de su evolución en el tiempo –mutaciones– las cuales les proveen resistencia a los medicamentos actuales, y también a la aparición de nuevos patógenos infecciosos. Es importante entender su estructura, función e interacciones a nivel molecular para tratar de desarrollar nuevos fármacos contra los patógenos actuales y los que puedan surgir en el futuro. C2
Bibliografía
- Acheson N. Fundamentals of Molecular Virology. John Willey and Sons. 2009.
- Abbas AK, Lichtman AH, Pillai S. Cellular and Molecular Immunology. Saunders Elsevier. 2010.
- Allaranga Y, Kone ML, Formenty P, Libama F, Boumandouki P, Woodfill CJ, Sow I, Duale S, Alemu W, Yada A. Lessons learned during active epidemiological surveillance of Ebola and Marburg viral hemorrhagic fever epidemics in Africa. East Afr J Public Health. 2010 Mar; 7(1): 30-6.
- De La Vega MA, Wong G, Kobinger GP, Qiu X. The Multiple Roles of sGP in Ebola Pathogenesis. Viral Immunol. 2015 Feb; 28(1): 3-9.
- Geisbert TW, Geisbert JB, Leung A, Daddario-DiCaprio KM, Hensley LE, Grolla A, Feldmann H. Single-injection vaccine protects nonhuman primates against infection with Marburg virus and three species of Ebola virus J Virol. 2009 Jul; 83(14): 7296-304.
- Paz de la Rosa G, Monroy-García A, Mora-García Mde L, Peña CG, Hernández-Montes J, Weiss-Steider B, Gómez-Lim MA. An HPV 16 L1-based chimeric human papilloma virus-like particles containing a string of epitopes produced in plants is able to elicit humoral and cytotoxic T-cell activity in mice. Viral J, 2009 Jan 6; 6:2.
- Petukhova NV, Gasanova TV, Ivanov PA, Atabekov JG. High-level systemic expression of conserved influenza epitope in plants on the surface of rod-shaped chimeric particles. Viruses. 2014 Apr 21; 6(4): 1789-800.
- Rosales-Mendoza S, Alpuche-Solís AG, Soria-Guerra RE, Moreno-Fierros L, Martínez-González L, Herrera-Díaz A, Korban SS. Expression of an Escherichia coli antigenic fusion protein comprising the heat labile toxin B subunit and the heat stable toxin, and its assembly as a functional oligomer in transplastomic tobacco plants. Plant J. 2009 Jan; 57(1): 45-54.
- Schiller JT and Davies P. Delivering on the promise: HPV vaccines and cervical cancer. Nature Reviews Microbiology. 2004 Vol 2 April: 343-347.
- Tomson TT, Roden RB, Wu TC. Human papillomavirus vaccines for the prevention and treatment of cervical cancer. Curr Opin Investig Drugs. 2004 (12): 1247-1261.
- Vaccine Technology V, Junio 8-13 2014.
- Warren TK, Wells J, Panchal RG, Stuthman KS, Garza NL, Van Tongeren SA, Dong L, Retterer CJ, Eaton BP, Pegoraro G, Honnold S, Bantia S, Kotian P, Chen X, Taubenheim BR, Welch LS, Minning DM, Babu YS, Sheridan WP, Bavari S. Protection against filovirus diseases by a novel broad-spectrum nucleoside analogue BCX4430. Nature. 2014 Apr 17; 508 (7496): 402-5.
- Zumbrun EE. Mission Critical: Mobilization of Essential Animal Models for Ebola, Nipah, and Machupo Virus Infections Vet Pathol. 2015 Jan; 52(1):18-20.

Mabel Castellanos -
Un articulo muy interesante para quienes queremos conocer mas sobre las vacunas y su historia
Juan R. -
Sin duda, un reporte muy completo, Felicidades a ambos investigadores !!!